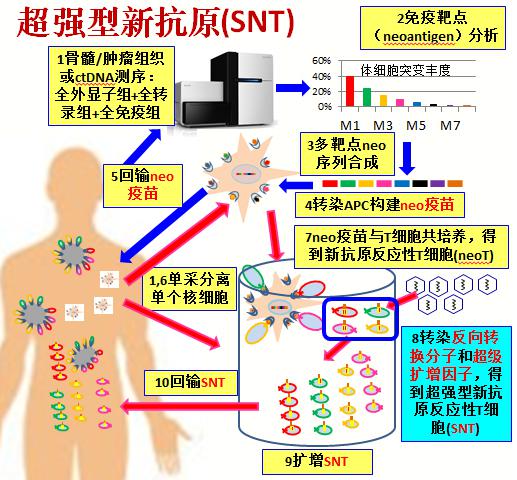
一、肿瘤基因时空全景测序,锁定neoantigen靶点
- 单靶点治疗存在严重局限性
- 低通量检测时代的技术局限带来的认识误区:
- 认为肿瘤是单个基因突变的结果,仅一个基因突变即可对肿瘤进行分子分型,如HER2阳性的乳腺癌,ALK阳性的肺癌,EGFR阳性的非小细胞肺癌等。这就好比盲人摸象,摸到什么就认为大象是什么,测到哪个基因的问题就说肿瘤是什么基因阳性,问题在于实验仅仅检测了这一个或极少数的基因。
- 认为对肿瘤的治疗,只需要对治单一靶标就OK,但实际上并不OK,大多数靶向药最终会耐药。
- 高通量检测时代的认知颠覆
传统达尔文理论推测,肿瘤里的突变应该不多,但NGS揭示的事实是:一个肿瘤里的突变数量可以高达108之多。
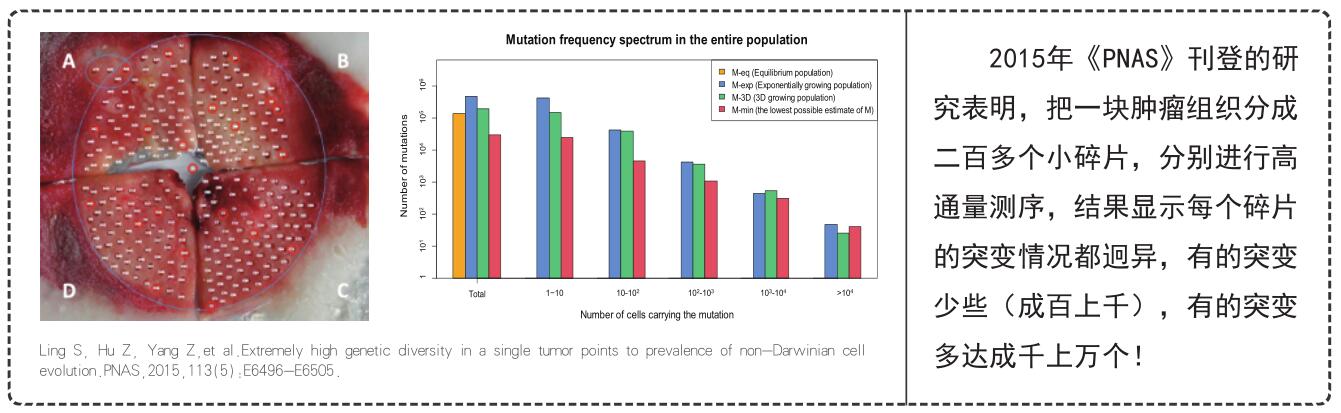
2015年《PNAS》刊登的研究表明,把一块肿瘤组织分成二百多个小碎片,分别进行高通量测序,结果显示每个碎片的突变情况都迥异,有的突变少些(成百上千),有的突变多达成千上万个!
- 因此肿瘤的基因组体现为突变谱,而非单一突变,其特点是:
- 静态看:突变的体细胞突变多达成百上千甚至上万
- 动态看:突变的丰度不断变化,新突变不断产生
- 个性化:每个患者的neoantigen都各不相同
- 单靶点治疗的局限
面对群狼(众多突变),只打一个能行?无论是靶向药,还是CAR-T,针对单靶点治疗,都会导致压力选择的结果,即“按下葫芦浮起瓢”——其他突变会大量滋生,导致耐药和复发。
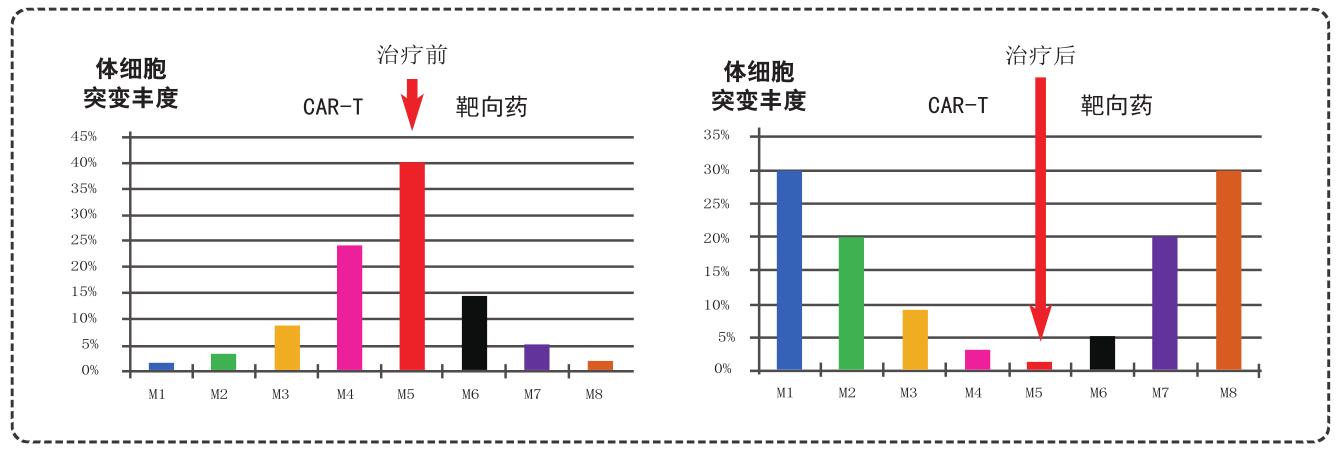
- 肿瘤基因时空全景测序,锁定neoantigen靶点
通过肿瘤新鲜组织全外显子组测序(WES)、肿瘤新鲜组织转录组测序(RNAseq)、HLA分型及抗原亲和力分析等项目,进行治疗靶标——新抗原(neoantigen)筛选。
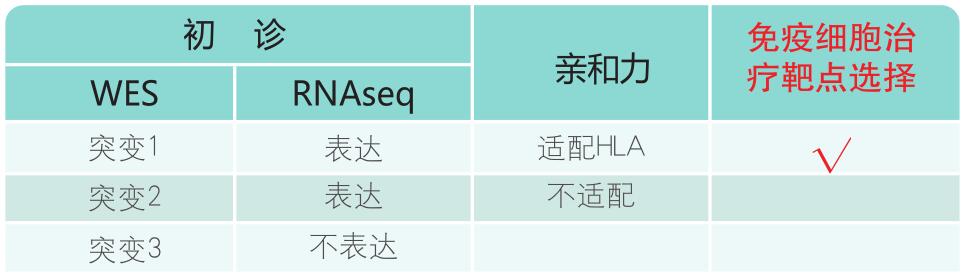
二、靶向neoantigen的个体化多靶点免疫治疗
卡替医疗将高通量基因测序与多靶点neo疫苗构建技术、T细胞免疫治疗技术相结合,开创了中国靶向新抗原(neoantigen)的个体化多靶点免疫治疗的先河。
- 新抗原治疗的细胞制备流程
- 免疫组、全外显子组、转录组及HLA测序获得肿瘤BCR/TCR、肿瘤体细胞突变及融合基因的新抗原信息。
- 新抗原负载抗原提呈细胞,制备负载新抗原的细胞疫苗(neoVx)。
- neoVx刺激T细胞,获得新抗原反应性T细胞(neoT)。将neoVx与neoT联合回输用于治疗。或进一步对neoT进行单细胞测序,获得肿瘤特异性TCR序列,制备TCR-T细胞进行治疗。即为普通型新抗原治疗技术。
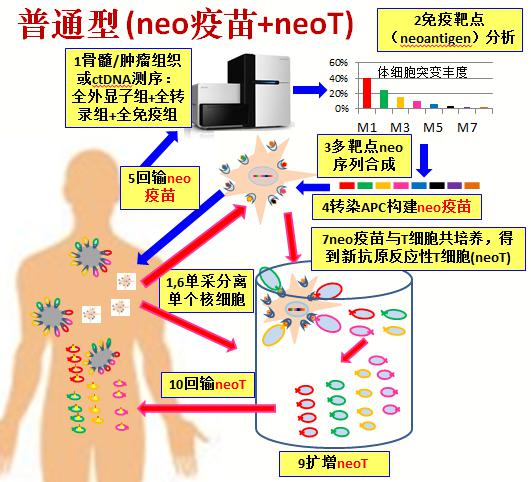
- 新抗原免疫治疗在血液肿瘤应用的意义
新抗原治疗可以解决CAR-T所无法解决的难题:
- 针对T细胞肿瘤患者的治疗
- 针对CAR-T无效或复发患者的治疗
- 与CAR-T联用以降低复发概率
- 血液肿瘤的新抗原的三类来源
- B/T系肿瘤细胞的BCR/TCR,来自免疫组测序(检测样本来自肿瘤组织或骨髓,或联合ctDNA);
- 肿瘤细胞的体细胞突变,来自全外显子组(检测样本来自肿瘤组织或骨髓,或联合ctDNA)及转录组测序(检测样本来自肿瘤组织或骨髓);
- 肿瘤细胞的融合基因,来自转录组测序(检测样本来自肿瘤组织或骨髓);
三、增强型和超强型新抗原技术
肿瘤免疫治疗必须解决以下三大难题:
- 难题1:如何让T细胞特异识别肿瘤?
- 难题2:如何让T细胞突破微环境障碍,杀伤肿瘤?
- 难题3:如何让可特异杀伤肿瘤的T细胞数量无限扩增?
前述新抗原疫苗及T细胞治疗技术仅仅解决了第一个难题,但后面两个难题会制约该技术的疗效。
- 什么是增强型的新抗原疗法?
增强型新抗原疗法是北京卡替医疗公司的原创专利发明,是在普通新抗原反应性T细胞(neoantigen reactive T cells,neoT)基础上,加入免疫检查点-共刺激分子的反向转换分子,制备增强型新抗原反应性T细胞(Enhanced neoT),将肿瘤微环境的抑制信号转换为T细胞的共刺激信号,从而巧妙的克服肿瘤微环境障碍,实现更强的肿瘤杀伤功能。
- 什么是超强型的新抗原疗法?
超强型新抗原疗法是北京卡替医疗公司的原创专利发明,是在增强型新抗原T细胞(ENT)基础上,进一步加上了超级扩增因子的基因修饰,使得ENT变成超强型neoT(SNT),从而能在体内自我复制扩增,突破细胞数量瓶颈,就像孙悟空拔一根毫毛能变成千上万个孙猴子能同时对抗十万天兵一样。超强型新抗原疗法的制备过程如下图。